慢病毒主要不良影响
1、插入诱变:慢病毒载体可以破坏细胞发育和增殖的正常调节,从而导致肿瘤发生;
2、转基因致癌作用:转基因是致癌基因,可在感染的细胞中诱导致癌作用;
3、产生具有复制能力的逆转录病毒:慢病毒载体可能会发生一系列低概率事件,从而恢复为具有复制能力的逆转录病毒;
提升慢病毒生物安全性的措施
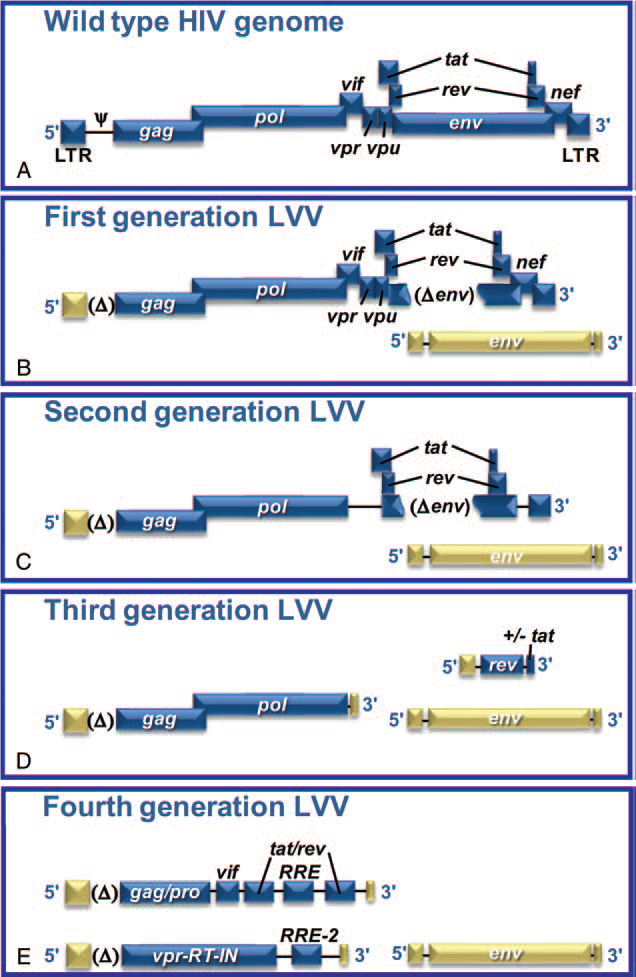
- 一代,二代,三代,四代慢病毒载体:第二代慢病毒载体删除了四个辅助基因vif,vpr,vpu和nef,而对载体产量或感染效率不影响,这些修饰同样达到了提高慢病毒安全性的目的,原因是任何具体复制能力的慢病毒都将缺少这些毒力因子。第三代和第四代慢病毒载体在此基础上更进一步的减少了产生具体复制能力病毒的可能性,将产生慢病毒的必须基因分别构建到了不同的载体上。
2、VSV-G:慢病毒载体设计的最早进展之一是用水泡性口炎病毒糖蛋白(VSV-G)基因取代了天然的HIV包膜基因,慢病毒载体的这种设计排除了野生型HIV的形成,即使在不太可能的情况下包装和转移质粒之间会发生重组。
3、自失活穿梭载体:删除位于转移载体3'LTR U3区域的启动子和增强子元件,在逆转录过程中,U3缺失从3'LTR复制到5'LTR,产生的具有U3修饰过的LTR的启动子活性只有原来的10%。这一修改改善了(并不是完全解决)慢病毒载体的大多数安全问题。
尽管一系列措施已经改善了慢病毒的生物安全性,但我们依然需要正确使用慢病毒。在实验室中,大部分慢病毒直接接触是通过接触完整皮肤而发生的。与HIV一样,慢病毒接触到完整的皮肤与临床无关,也不会构成重大风险。与临床相关的接触是通过肠胃外接种,与眼睛,鼻子或嘴的粘膜接触或直接与不完整的皮肤接触。防止接触的最佳方法是适当的技术,培训和个人防护设备。这将包括仔细检查在实验中使用锐器的可能性,并在可能的情况下消除这种可能性。在实验室环境中同样可能会间接接触液滴或较小的空气传播颗粒,通过飞沫传播的气溶胶暴露是间接接触慢病毒的另一种潜在途径。

文章“Risks Associated With Lentiviral Vector Exposures and Prevention Strategies”总结了几点自我应急处理措施,列举如下:
完整皮肤接触:立即用大量自来水冲洗接触的区域,以稀释,清洁并冲洗完整皮肤上的慢病毒。
非完整皮肤接触:立即用大量肥皂和水冲洗接触的区域,以稀释,清洁并冲洗该区域的慢病毒。
粘膜接触[眼睛,鼻子或嘴]:立即用流水冲洗该区域至少15分钟。
安全生产最重要。如果需要立即就医,请致电急救人员。稳定受伤人员并为需要立即就医的伤害提供急救,例如深切,出血等。同时根据具体情况可以考虑提供以下治疗:尽快但在72小时内,开始7天的NRTI(例如替诺福韦)和整合酶抑制剂(例如raltegravir或dolutegravir)疗程,观察和处理接触事件的明显影响。
在这里说下被注射慢病毒的针或者注射器扎伤的情况。理想情况下,建议在针刺伤后1小时内进行暴露后预防(post-exposure prophylaxis,PEP),以最大程度地降低发展HIV血清阳性的风险。抗病毒药(例如AZT)可有效抑制病毒逆转录酶从病毒RNA形成DNA拷贝,以在使用潜在有害的转基因时最大程度地减少与无意转导相关的生物危害。PEP治疗需要由职业健康医生开具处方,因为抗逆转录病毒药物的耐受性通常不高,因此,其必须根据暴露的严重程度以及与表达的转基因相关的生物危害性来确定是否需要治疗。
文章内容就介绍到这里,更多关于慢病毒安全生产,安全使用的介绍可以阅读如下两篇文章:
Rothe M, Modlich U, Schambach A. Biosafety challenges for use of lentiviral vectors in gene therapy. Curr Gene Ther. 2013;13(6):453–468. doi:10.2174/15665232113136660006;
Sinn PL, Sauter SL, McCray PB Jr. Gene therapy progress and prospects: development of improved lentiviral and retroviral vectors--design, biosafety, and production. Gene Ther. 2005;12(14):1089–1098. doi:10.1038/sj.gt.3302570.
